チタンやタンタルは、軽微な腐食でも注意おこたるべからず
チタン、タンタル、ジルコニウムなどのリアクティブメタルと呼ばれる金属を化学プランの装置材料として用いる際に、腐食速度0.1mm/年以下の軽微な全面腐食をともないつつ使用される場合がある。その腐食速度自体は構造材料として許容される範囲であっても、腐食反応にともなう水素を吸収し水素脆化(1)の発生可能性がある。
その原因は、腐食反応の進行にともない金属表面で水素発生が生じ、その水素の一部をチタン等が吸収し、固溶水素もしくは金属水素化物を形成し脆化するためである。水素脆化が進行すると、応力状態により脆性破壊の発生する危険性がある。
ただし、例外として高温硝酸環境中でチタンを使用する場合などで、その場合のカソード反応は、水素発生反応でなくNO3イオンの還元反応などであるため、全面腐食が発生しても水素脆化は発生し難いこともある。
チタンやタンタル中の水素濃度は、サンプルの機器分析(2,3)で評価できる。このため、全面腐食が認められて場合は、実機よりサンプルを採取するか、その環境に浸漬した試験片を用いて水素分析を行うことが可能である。チタンやタンタルで水素濃度が100ppmを超えた場合には、水素脆化による破壊が生ずる可能性がある。この場合は、他の金属での更新を検討する必要がある。
なお、脆化しても破壊するかどうかは、部材への応力の大きさや、ひずみ速度に依存する。水素濃度100ppmは、負荷される応力が高いとか変動速度が大きい場合を想定した、やや安全側の限界値である。
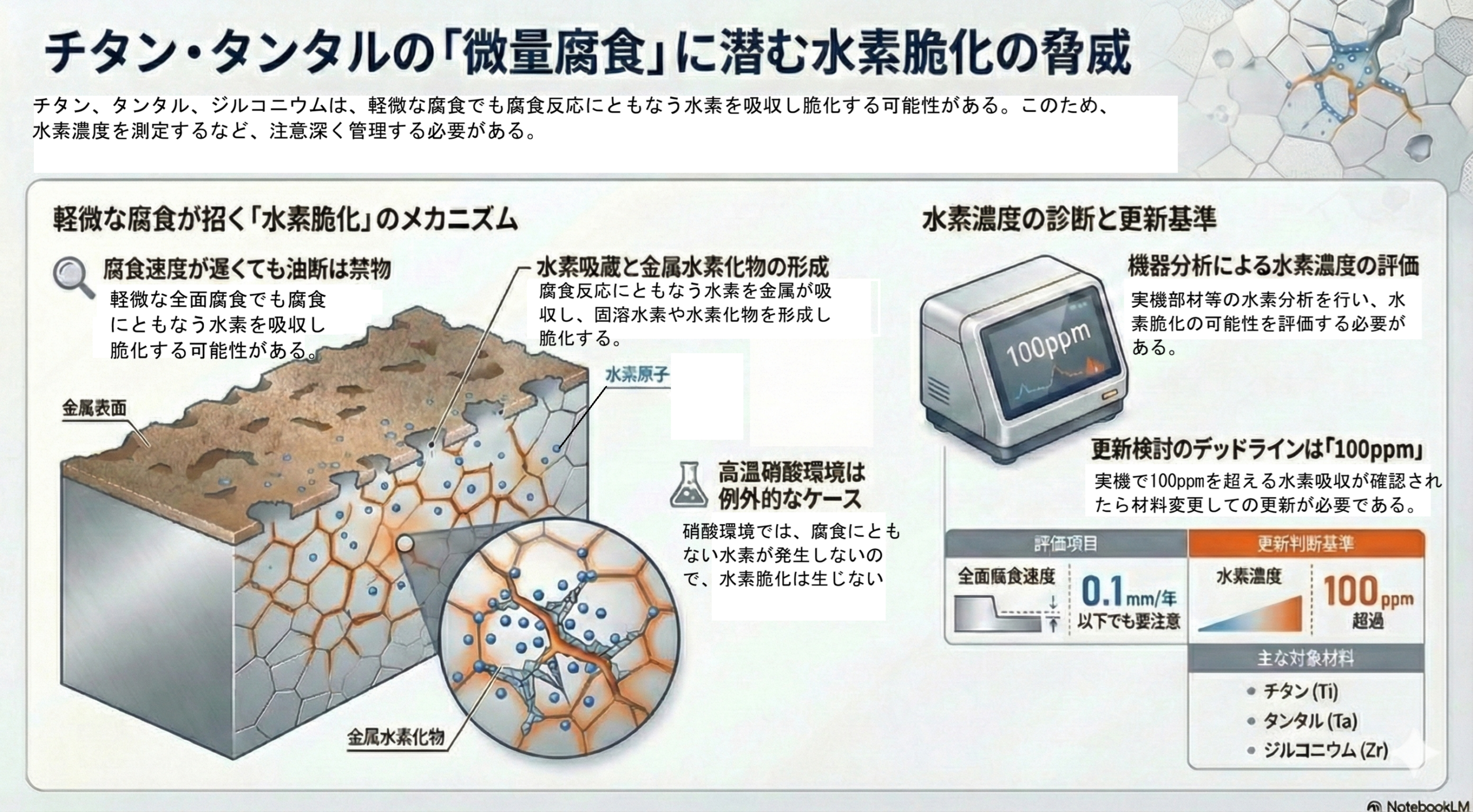
図 チタンやタンタルの腐食にともなう水素脆化の危険性
参考資料
(1) 中原正大、「事例に学ぶ 化学プラントの材料損傷とその制御」、アマゾン、P.110、(2024)
(2) JIS H 1619:2012 チタン及びチタン合金−水素定量方法
(3) JIS H 1696:2000 タンタル中の水素定量方法
この記事は、会員専用記事です。
会員になると、会員専用の記事もお読みいただけます。